高淑萍医生的科普号
- 精选 妊娠期糖尿病分娩期及产后管理
GDM患者及其后代均是公认的糖尿病的高危人群,GDM患者产后患2型DM的危险明显增加。 分娩时机 1.不需要胰岛素治疗而血糖控制达标的GDM孕妇,无母、儿并发症的情况下,严密监测下,可等到预产期,仍未自然临产者采取措施终止妊娠。 2.孕前糖尿病及应用胰岛素治疗的GDM者,如果血糖控制良好,无母、儿并发症的情况下,严密监测下,孕39周后终止妊娠;血糖控制不满意者或者出现母、儿并发症,及时收入院密切母儿并发症,终止妊娠时机采取个体化处置。 3.糖尿病伴发微血管病变者,或者以往有不良产史者,在严密监护下,终止妊娠时机需要采取个体化处置。 分娩方式 糖尿病本身不是剖宫产的指征,决定阴道分娩者,应制定产程中分娩计划,产程中密切监测孕妇血糖、宫缩、胎心变化,避免产程过长。 选择性剖宫产手术指征有糖尿病伴严重微血管病变及其他产科指征。孕期血糖控制不好,胎儿偏大尤其估计胎儿体重在4250g以上者或既往有死胎、死产史者,应适当放宽剖宫产指征。 分娩期及围手术期胰岛素的使用原则 使用原则 手术前后、产程中、产后非正常饮食期间停用所有皮下注射胰岛素,改用胰岛素静脉滴注,避免出现高血糖或低血糖。供给足够葡萄糖,以满足基础代谢需要和应激状态下的能量消耗。供给胰岛素以防止DKA的发生,控制高血糖,并有利于葡萄糖的利用。保持适当血容量和电解质代谢平衡。 产程中或手术前的检查 必须测定血糖、尿酮体。选择性手术还要行电解质、血气、肝肾功能检查。 胰岛素使用方法 每1~2h监测血糖,根据血糖值维持小剂量胰岛素静脉滴注。孕期应用胰岛素控制血糖者计划分娩时,引产前一日睡前中效胰岛素正常使用;引产当日停用早餐前胰岛素;给予静脉内滴注生理盐水;一旦正式临产或血糖水平减低至3.9 mmol/L以下时,静脉滴注从生理盐水改为5%葡萄糖液并以100~150ml/h的速度输注,以维持血糖水平大约在5.6mmol/L左右;若血糖水平超过5.6mmol/L,则采用5%葡萄糖液,加短效胰岛素,按1~4U/h的速度静脉输注;血糖水平采用快速血糖仪每小时监测1次,调整胰岛素或葡萄糖输注的速度。也可按照下表的方法调控血糖。 妊娠合并DKA的处理 临床表现及诊断 恶心、呕吐、乏力、口渴、多饮、多尿,少数伴有腹痛;皮肤黏膜干燥、眼球下陷、呼气有酮臭味,病情严重者出现意识障碍或昏迷;实验室检查显示高血糖(>13.9mmol/L)、尿酮体阳性、血PH16.6mmol/L),胰岛素0.2~0.4U/kg一次性静脉注射。 (2)胰岛素持续静脉滴注:0.9%NS+RI,按胰岛素0.1U/kg/h或4~6U/h的速度输入。 (3)监测血糖,从使用胰岛素开始每1h监测一次血糖,根据血糖下降情况进行调整,要求平均每小时血糖下降3.9~5.6mmol/L或超过静脉滴注前水平的30%。达不到此标准者,可能存在胰岛素抵抗,应将RI加倍。 (4)当血糖降至13.9mmol/L时,将0.9%NS改为5%的葡萄糖液或葡萄糖盐水,每2~4g葡萄糖加入1U胰岛素,直至血糖降至11.1mmol/L以下、尿酮体阴性、并可平稳过渡到餐前皮下注射治疗时停止补液。 注意事项 补液原则先快后慢、先盐后糖;注意出入量的平衡。开始静脉胰岛素治疗和患者有尿后要及时补钾,避免严重低血钾的发生。当PH
高淑萍 主治医师 安徽省妇幼保健院 产科5562人已读 - 就诊指南 孕期补钙(转载)
最近在看门诊时,经常会被问到孕期补钙的问题,集中起来一并回答如下: 1. 每个孕妇在进入妊娠中晚期以后都要补钙吗? 是的,绝大多数孕妇都需要额外补充钙。从孕早期的一个受精卵发育到一个足月的孩子,需要很多的钙来帮助孩子长骨骼和牙齿。根据膳食调查,我国女性在孕期的每日钙摄入量大约为300-400mg,即使是在钙摄入量比较多的西方女性,孕期的每日平均钙摄入量也只有800mg左右,均低于妊娠中晚期每日推荐的1000-1200mg的钙摄入量。如果每天食用的食物中有很多的牛奶和奶制品(例如酸奶和奶酪),是可以不需要额外补钙的,但是绝大多数人是做不到的。 2. 补钙的同时要补维生素D吗? 是的,维生素D的一个主要作用是帮助钙的吸收和利用,如果在补充钙的同时不补充维生素D的话,钙的吸收和利用会受到一定的影响。另外,维生素D对于母亲和孩子的皮肤和视力也有额外的好处。 3. 有哪些钙的制剂比较好一些? 多数钙剂的吸收率基本上差不多,所以不要相信那些广告中夸大其词的骗人鬼话,重要是钙制剂中钙元素的含量是真实的,还有钙制剂的生产工艺是有安全保障的。 4. 在进入妊娠中晚期后经常出现腿抽筋是缺钙引起的吗? 妊娠中晚期腿抽筋的主要原因是钙缺乏,补充钙剂会缓解该症状。但是腿抽筋还有其他的原因,例如血供不足和疲劳等,这也是为什么有些人吃了钙片还会腿抽筋的原因。 5. 妊娠晚期继续补钙会不会造成胎儿头太硬,生不出来? 明显缺钙时胎儿的头会比较软,但是多吃了钙并不会造成胎儿头太硬,根本没有必要担心胎儿头硬或双顶径比较大生不出来。和成人不一样的是,胎儿的颅缝没有闭合,在产道的挤压下,胎儿的颅缝可以重叠,双顶径变小,从而顺利地从阴道分娩。所以经阴道分娩的孩子的头往往是“长长的”,过了几天就变得“圆圆的”了。 6. 听说补钙会让胎盘老化? 第一:补钙不会造成胎盘老化。第二:所谓的“胎盘老化”和孩子的出生以及预后之间没有必然的联系。
高淑萍 主治医师 安徽省妇幼保健院 产科1719人已读 - 就诊指南 写给妊娠期糖尿病的孕妇(转载)
对于女性来讲,怀孕是一段充满了未知的旅程,是一种期待,也是一种挑战,我曾经杜撰了一个词:PCT(Pregnancy Challenge Test,妊娠挑战试验)。如果妊娠期出现某一个器官或系统的问题的话,进入40-50岁以后,这个器官或系统出问题的概率或风险会明显上升,GDM就是一个很好的案例。 目前推荐每一位孕妇都要在孕中期进行GDM筛查,因为很多在非孕期血糖正常的女性怀孕以后会出现糖代谢的异常。近些年,由于GDM诊断标准的变化导致了其发生率明显上升。在采用新的诊断标准之前,国人GDM的发生率大约为5%,实施新标准以后,GDM的发生率一下子跳升到18%左右。当然,在不同的区域,这些数据会略有不同。 调整GDM诊断标准的目的不是让1/5的孕妇都成为病人,是为了给大家一个警示,是为了提醒大家需要调整生活方式,是为了让大家预防可能发生的近期和远期不良结局。 被诊断为GDM以后,有的人很紧张,专门去买血糖仪在家每天监测空腹和餐后血糖;有的人无所谓,随便你医生怎么说,我该干嘛还是干嘛。其实,对于GDM,科学合理的做法是:要重视,但是不必过于担心,多数通过饮食调整和适量运动就可以得到很好的控制。 GDM对母亲和孩子的近期影响与远期影响 理论上讲,GDM会导致巨大儿的发生率升高,围产儿并发症和死亡率也会升高,还会导致其他母体并发症的发生率上升。但是,在多数情况下,GDM母儿的近期结局是良好的,因为真正血糖控制不好的孕妇还是少数。 GDM孕妇在分娩以后,绝大多数血糖会恢复到正常状态,但是如果不注意进行饮食调整和适量运动的话,未来患II型糖尿病的概率会明显上升。研究数据显示,与没有GDM的女性相比,有GDM女性未来患II型糖尿病的风险会升高5-10倍,在未来的5-10年内,患II型糖尿病的概率为30-50%(不同的研究会有不同的数据)。 对于GDM孕妇来讲,控制血糖水平不仅仅是为了减少对自身和胎儿的近期不良影响,更重要的是减少对子代的远期不良影响。因为宫内的高糖环境会对子代的糖代谢产生不良影响,这种不良影响会随子代年龄的增加而越发显著。其子代在20岁时患II型糖尿病的累积风险接近15%,24岁时增加到30%以上,并且这种增加的程度与母亲妊娠晚期时的血糖水平呈正相关。 GDM孕妇自我管理的建议 如果你去看糖尿病专科医生/GDM专家或者是营养专家的话,除了定期监测血糖以外,TA们会给你很多很详细的专科建议和很多的食谱选择和建议。这些建议很专业,也都有很多的科学依据和循证医学证据,还有很专业的计算公式和海量的食谱来帮助你选择和调整。 但是面对这些系统、全面、科学的要求,很多的“糖妈妈”无法做到,这让专家和“糖妈妈”都很无奈,很受伤。其实,对于大多数的GDM孕妇来讲,并不需要去找专科医生或营养专家,只要你能遵守我以下的自我管理建议,多数能获得很好的结果。如果你按照我的“傻瓜”建议去做了,还是无法很好地控制血糖和体重的增加,那你就乖乖地去看专科医生吧。 管住嘴 对于GDM孕妇来讲:蔬菜类原则上可以放开,想吃多少吃多少;蛋白质的摄入要适量,不过量。如果对肉类和海鲜类一点也提不起兴趣,可以适当进食奶制品或蛋类;要控制的主要是碳水化合物类,包括主食、点心和含糖分的饮料。 吃饭不要吃十分饱,八分饱就差不多了,为了减少饥饿感,改一日三餐为一日四餐,要少食多餐。最好能戒掉甜点和含糖饮料,水果也不能多吃,要吃的话尽量吃含糖量少的水果(下次我会专门写一篇文章“都是水果惹的祸”)。 迈开腿 除了控制饮食以外,最好还要能迈开腿,要保证每天一定的运动量。对于孕妇来讲,最简单最安全的运动方式是走路,每天或者隔天能走路30-60分钟。刚开始的时候可以散步,然后根据自身的情况逐步过渡到快步走,有效运动的标准是心跳要有明显加快的感觉,要有出汗的感觉。当然要以安全为前提,运动不要让自己不适,不要引起明显的宫缩,一般的生理性宫缩不要紧。 控制目标 通过运动和饮食控制,最好能做到三个“达标”:血糖达标、自身体重增加达标、胎儿体重增加达标。在妊娠中晚期,不建议每周体重增加超过一斤,对于一些超重或肥胖的GDM妈妈,可能会要求每周体重增加不能超过半斤;孩子的出生体重最好能控制在6斤左右。 饮食日记 对于自控能力比较差的GDM妈妈,或者是控制效果不太好的GDM妈妈,需要认真地每天写饮食日记。也就是说要把你每天吃的每一口食物及饮料都要纪录下来,并同时纪录你的体重增加情况和血糖检查结果。 写饮食日记有两个用处,一是给自己看,你会发现你吃的往往会比你自己认为的多很多,这样第二天你就要把多吃的东西减掉。二是给医生看,医生会根据你的情况给予科学合理的建议。 你应该知道的GI和GL GI(GlycemicIndex)指的是“血糖生成指数”,是反映食物引起人体血糖升高程度的指标,简单来说,越容易使血糖快速上升的食物,其GI值就越高。例如葡萄糖的GI值=100,GI>70的食物为高GI食物,GI
高淑萍 主治医师 安徽省妇幼保健院 产科3092人已读 - 医学科普 2016阻断乙肝母胎垂直感染
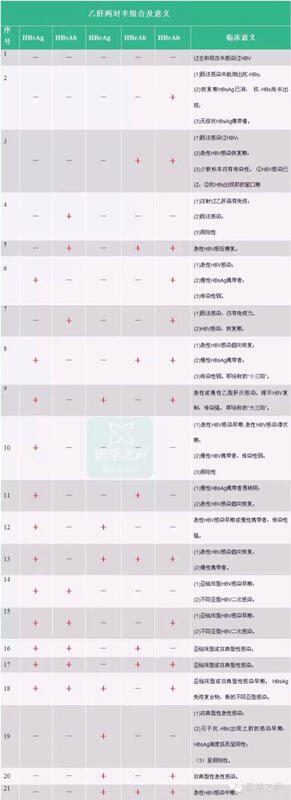
2016 SMFM,AJOG发布阻断乙肝母胎垂直感染最新指南 1、孕期常规筛检 HBsAg (1A) 2、HBsAg(+):产后12小时内,给予新生儿乙肝疫苗及HBIG (1A) 3、HBsAg(+):晚孕期测乙肝病毒量(2B) 4、HBsAg(+),乙肝病毒量>6-8 log10copies/mL:考虑孕期抗病毒治疗(2B) 5、孕期抗病毒治疗首选:tenofovir (2B) 6、给予新生儿乙肝疫苗及HBIG后,即可母乳哺育(1C) 7、乙肝病毒量>7 log10 IU/mL可能增加产前诊断措施(羊水穿刺、绒毛取样)导致之垂直感染风险(2C) 8、乙肝带原非剖腹生产适应症(2C)
 高淑萍 主治医师 安徽省妇幼保健院 产科4910人已读
高淑萍 主治医师 安徽省妇幼保健院 产科4910人已读 - 医学科普 如何解读甲状腺功能检查化验单
如何解读甲亢的化验单 2016-01-02 中华检验医学网 检验医学 典型的甲亢病人,不用化验甲状腺功能就可诊断,上世纪70年代以前就是这样的。但是对甲状腺无明显肿大的不典型病人或老年人,若不作甲状腺功能化验,就很难确诊。故甲状腺功能检查已成为甲亢诊断,疗效判定,甲亢复发,停药指标的重要参考内容。 甲状腺功能化验内容主要包括如下几项: 1.甲状腺素分泌指标 如血清总T3(TT3)、总T4(TT4)、游离T3(FT3)、游离T4(FT4)。分泌指标高低直接反应甲状腺的功能状态,增高表示功能增进,减少表示功能减低。T3、T4在妊娠、服避孕药、雌激素治疗等情况下可增高;在雄激素和强的松治疗、肾病综合征、肝功衰竭、服用苯妥英钠和保泰松时可减低,故对甲亢诊断准确性受到限制。但FT3、FT4不受上述因素影响,是目前诊断甲亢、甲减的常用化验指标。但是多数医院常将TT3、TT4、FT3、FT4一起检查。FT3占总T3的0.3%,FT4占总T4的0.04%,含量虽然少,但生物活性极高,因为只有游离T3、T4才能进入细胞内,起到生理作用。FT3在甲亢早期或复发初期最先升高,对甲亢诊断意义大,而FT4甲亢时也增高,但甲减时最先降低,对甲减诊断优于FF3。反T3(rT3):95%以上由T4在周围组织代谢时脱碘形成,不具生理活性,对甲亢诊断意义不大,它在甲亢时与T3、T4、FT3、FT4同步升降,只是在甲亢或甲亢复发的早期先期升高,而且在非甲状腺疾病,T3、T4、FT3、FT4正常时,rT3可以独立升高。T3、T4在甲亢时常同步升高,但也有例外: (1)仅T3增高:①T3型甲亢:在缺碘地区多见。②T3优势甲亢:甲亢经药物治疗后,T4已正常,而T3持续不降甚或增高,T3(纳克/毫升)/T4(微克/毫升)>30,此型复发率高,宜手术治疗。③甲亢早期或甲亢复发初期。4甲减用甲状腺片治疗时。正常甲状腺组织是按照T31:T49的比例分泌的,而甲状腺片中的T3为11而T4为12,含量近乎相等,而且T3吸收率95%,T4仅40%,长期服用会出现T3增高的现象。故现在提倡用左旋甲状腺素钠(优甲乐),可避免T4不足。 (2)仅T4增高:①T4型甲亢:与吃含碘食物过多有关,②假性T4甲亢:常见于心梗、肺心病、急性脑血管病、哮喘、肿瘤、急性肝病等,随着原发病好转而下降。③少数老年甲亢,可仅T4高。 (3)T4减低:①见于甲减②慢性心、肺、肝、脑疾病。 2.促甲状腺激素(TSH) 在脑垂体产生,有促进甲状腺滤泡细胞产生T3、T4、FT3、FT4的作用。它的高低受甲状腺素负反馈控制,其表现是相反的,甲状腺素高时,TSH低;甲状腺素低时,TSH高。故甲亢时T3、T4、FT3、FT4增高,而TSH是降低的,甲减时相反。
高淑萍 主治医师 安徽省妇幼保健院 产科3544人已读 - 学术前沿 剖宫产术后子宫瘢痕妊娠继发早期胎盘植入的诊断及临床处理
随着剖宫产率的上升,随之而来的诸多临床问题也越来越受到关注,如子宫破裂、前置胎盘、胎盘植入、剖宫产术后子宫瘢痕妊娠(cesarean scar pregnancy, CSP)、不孕、腹腔内脏器粘连等。其中,CSP作为剖宫产术后妇女再次妊娠的重要早孕期并发症之一,成为常见的新型妇产科急危重症。CSP是指孕囊植入在前次剖宫产子宫瘢痕处或形成的憩室处,故可以认为是一种特殊类型的异位妊娠。作为剖宫产的一种远期并发症,其诊断和治疗方面迫切需要明确统一的指导性意见。CSP已经成为一种“新型的疾病”受到前所未有的关注,国内外相关学术文章发表的数量持续上升。文章的类型也从早期的个案报道,到最近越来越多病例数的系列研究。在我国剖宫产率居高不下的历史背景下,CSP的发病情况可能尤为严重,因此,更迫切地需要学者们继续深入研究和总结,制定符合我国特点的行业规范,以提高CSP的诊疗水平和围产保健工作质量。本文着重介绍CSP中后果最为严重、处理也最为棘手的一个问题,即早孕期CSP继续发展形成的凶险型前置胎盘伴胎盘植入,并且本文讲解的重点不是阐述妊娠后半期的胎盘植入,而是与CSP相关的、早孕期和中孕早期胎盘植入的相关问题,以便加强临床工作者对这一严重产科合并症的了解,在临床上能尽早进行识别并恰当地处理。 ◆ ◆ ◆ ◆ ◆ 一、CSP是胎盘植入的早期病变 随着有剖宫产史育龄期妇女的人数增多,胎盘异常植入(粘连性胎盘、植入性胎盘、穿透性胎盘)患者数也明显上升。本文用“胎盘植入”代表上述3种胎盘异常植入。美国的数据显示:1930—1950年,胎盘植入是很罕见的,发生率为1/30 000 产次;到1950—1960 年,发生率为1/19 000 产次;到了20世纪80年代,则升至1/7 000产次;1994—2002年,发生率则上升达到1/2 500~1/2 000产次;2010年后,估计达到了1/333产次[1-3]。有学者认为,CSP的发生率上升与剖宫产率升高关系密切。 此外,对于同为剖宫产远期并发症的CSP与胎盘植入,随着剖宫产率的增加,二者的发生率均在增加,故推测胎盘植入与CSP之间也存在密切联系[4]。胎盘植入和CSP有共同的病理学基础。二者都是滋养细胞在子宫瘢痕处种植,并侵入肌层。多次剖宫产的患者中胎盘植入的风险明显升高。高分辨率超声检查显示,在CSP很早期即有绒毛滋养细胞位于子宫瘢痕憩室深处。胎盘绒毛穿过尼氏层(Nitabuch layer)的蜕膜进入子宫瘢痕内。另有研究显示,胎盘附着于子宫瘢痕处,局部的缺氧应激环境会刺激细胞滋养细胞进一步侵入肌层深部。较之子宫内膜细胞,滋养细胞对细胞外基质的亲和性更高,这一现象可以解释为何巨噬细胞更趋向暴露的无细胞成分覆盖的瘢痕组织[5]。剖宫产术后形成的子宫瘢痕憩室,对CSP的发生应该有诱发作用。这一解释与临床相符,胎盘植入的位置多发生于手术后的子宫瘢痕处;剖宫产次数越多,CSP和胎盘植入的机会越大。当然,胎盘植入的发病也有其他方面的原因,但共同的特点是滋养细胞在蜕膜缺失的子宫腔表面侵袭能力增加,刮宫、剖宫产术、人工剥离胎盘、宫腔感染及子宫手术史都可能导致局部蜕膜缺失,诱发胎盘的异常植入。 Timor-Tritsch 等[5]报道了10例早孕期诊断为CSP患者的妊娠结局,结果10例患者最终均切除子宫,病理均证实为穿透性胎盘植入,且与CSP有共同的病理学特征。作者用“早期胎盘植入”来描述CSP继发的此类情况,与通常在晚孕期发现的胎盘植入相区别。进而有学者认为,CSP就是胎盘植入的先期病变,最终必然导致胎盘植入[6]。从CSP至胎盘植入是一个连续的疾病过程;通常,前者被限定于早孕期,而后者则针对中、晚孕期。二者尽管临床表现有所差别,但病理学机制是相同的。但迄今为止,世界范围内对二者尚无定义上的明确划分,在临床使用和文章发表中均缺乏统一标准。 二、CSP继发的早期胎盘植入的临床特点 CSP继发的早期胎盘植入会造成两个严重的后果,即自发性子宫破裂和因胎盘植入到剖宫产子宫切口导致的大出血。 更为重要的是,与一般的胎盘植入不同,此类CSP继发的早期胎盘植入在早孕期和中孕早期即出现症状,甚至导致危及生命的临床后果。Timor-Tritsch等[5]报道的10例CSP继发早期胎盘植入患者中,9例均在足月或接近足月时行择期剖宫产术,1例在孕20周时因突发阴道大量出血而急诊开腹切除子宫;所有患者均切除了子宫,2例术前在髂内动脉放置球囊协助压迫止血,但尽管如此,仍大量出血。 几乎所有的出血都源于新生血管与盆腔内脏器的粘连。胎盘剥离过程中出现的大出血较常发生,但少数情况下也会发生自发性子宫破裂。 Timor-Tritsch和Monteagudo[4]总结文献报道的47例早孕期和中孕早期发生胎盘植入的患者,其中15例发生自发性子宫破裂,腹腔内出血需开腹探查、子宫动脉栓塞、甚至切除子宫;子宫破裂的平均孕周为18.1周。有学者提出,早孕期发生的子宫破裂几乎无一例外是源于滋养细胞侵入子宫瘢痕处[6]。可以推测,原本已经很薄的子宫瘢痕肌层,由于滋养细胞继续侵入使其更加薄弱,这可能是早孕晚期或中孕早期发生自发性子宫破裂的主要原因。当然无瘢痕的子宫如果存在胎盘植入,也可能发生自发性破裂,但瘢痕处植入胎盘的子宫破裂风险更高。 上述早期胎盘植入可能发生的严重后果,使得产科合并症诊断的方案需要进行改变。对胎盘植入早期且可靠的诊断、了解病史、并知晓大多数是胎盘植入在前次剖宫产子宫瘢痕的位置,都使得对胎盘植入的关注时间提前至早孕期或中孕早期。 三、CSP继发早期胎盘植入的诊断 诊断早期胎盘植入和CSP是很困难的,可能会误诊为子宫下段妊娠、宫颈妊娠或流产。但有学者认为,子宫瘢痕处孕囊植入可能是胎盘植入最早期能通过超声发现的临床证据。 Timor-Tritsch等[5]报道的10例CSP继发早期胎盘植入患者的早孕期(孕5周+4~9周+2)影像学诊断标准为: (1)宫腔内空虚;(2)胎盘或孕囊位于子宫切口瘢痕缺损内或其上;(3)对于8孕周时则呈圆形或椭圆形;(4)孕囊与膀胱之间的肌层变薄(1~3 mm),甚至消失;(5)宫颈管闭合或空虚;(6)可见胎芽及卵黄囊,有或没有胎心;(7)妊娠试验阳性时,子宫瘢痕内或其上血流丰富。这10例患者在中晚孕期的超声检查即显示典型的胎盘植入征象。 Ballas等[7]对孕中期、晚期病理诊断为胎盘植入患者的早孕期超声特点进行回顾性分析,提出以下几点高危特征:前置胎盘、胎盘区域无回声、子宫肌层界限异常,这些征象如果早孕期出现,则应警惕胎盘植入;孕囊位置低也常伴随出现。Stirnemann等[8]进行前瞻性研究,对有剖宫产史的孕妇在孕11~14周的超声特点进行分析,根据子宫瘢痕与滋养细胞的关系判断是否为胎盘植入高危,将子宫瘢痕暴露于子宫腔并位于孕囊最低点的上方、孕囊占据宫颈管的偏上部分、同时有低置胎盘覆盖确定为高危;如果子宫瘢痕被保护包裹在宫颈管内,而滋养细胞未覆盖宫颈内口则视为低危;患者中晚孕期胎盘植入的超声特点为:胎盘后血窦(多普勒超声显示胎盘后有不规则血管流空区域)、胎盘后没有清晰的界限、胎盘覆盖的肌层变薄、膀胱界限中断、胎盘突入膀胱内、多普勒显示血流丰富[9-10]。该标准下的高危患者胎盘植入的发生率为9%~44%。MRI也能辅助发现胎盘植入,但这些检查的准确性和敏感性仍不得而知[11-12]。有相当一部分胎盘植入直到终止妊娠时才被发现,胎盘植入的诊断可以是剖宫产术中的临床诊断,也可以是切除子宫后的病理诊断,更可能伴随严重并发症的发生[13-15]。 四、早孕期CSP必然会发展为胎盘植入吗? 早期诊断为CSP的患者中,很少有采用期待治疗者,因此,目前对于CSP的自然病程仍不清楚。Timor-Tritsch等[5]提供的组织学证据显示,CSP在中孕期会发展为胎盘植入,因而提示CSP即是胎盘植入的早期病变。但文献报道的CSP结局很可能存在偏倚,因为只有出现严重临床后果的病例才予以报道,而其他预后良好的病例则未予体现。 Vial等[16]认为,CSP有两种类型,一种是孕囊种植在前次剖宫产子宫瘢痕处,但后续向宫颈管或宫腔内生长,这种胎儿常能够存活,但可能有大出血的风险;另一种即是孕囊深入种植在剖宫产子宫瘢痕缺损处,并向膀胱和腹腔方向生长,更容易发生子宫自发性破裂。也就是说,异常位置种植胎盘的深度和发展方向是决定CSP进程和结局的主要决定因素。但有学者认为,早期CSP即预示着滋养细胞的异常侵入,疾病未来的发展方向难以预测。有些学者拟将CSP 区分为“ 瘢痕之上”和“ 憩室之内”两种[17-19]。但Timor-Tritsch等[5]认为,这二者后续的胎盘均会种植在瘢痕处、锚定在瘢痕处,并侵入至肌层内、甚至穿透子宫浆膜层和膀胱,而随着孕囊的增大,都会向宫腔内膨出,而无所谓“瘢痕之上”和“憩室之内”。根据CSP自然病程的发展,区分二者对后续的处理并无帮助。CSP就是胎盘植入的早期病变。 此外,有学者认为,滋养细胞覆盖子宫瘢痕,并非胎盘植入发生的唯一高危因素。Stirnemann等[8]的资料显示,有≥1次剖宫产史的孕妇中,5.8%的孕妇于孕12周时的超声征象符合胎盘植入高危的类型。Miller等[20]研究显示,对于有1次剖宫产史的患者,胎盘植入在
高淑萍 主治医师 安徽省妇幼保健院 产科5498人已读 - 医学科普 妊娠合并甲减诊治规范
一、诊断妊娠期甲状腺功能异常,应建立本单位或地区的血清甲状腺功能指标参考值 二、目前可应用2011年美国甲状腺疾病学会(ATA)推荐的正常值 早期TSH 0.1~2.5 mIU/L 中期TSH 0.2~3.0mIU/L 晚期TSH 0.3~3.0mIU/L 三、甲状腺疾病高危人群: 1.甲状腺疾病史、甲状腺手术史、碘131治疗史 2.甲状腺疾病家族史 3.甲状腺肿大 4.甲状腺自身抗体阳性 5.有甲减或甲减的症状及临床表现 6.I型糖尿病 7.其他自身免疫病 8.不孕妇女 9.曾有头颈部放疗 10.肥胖症(BMI大于40) 11.30岁以上妇女 12.服用胺碘酮治疗,最近碘造影剂暴露的妇女 13.流产、早产史 14.居住在碘缺乏区妇女 四、临床甲状腺功能减退症 妊娠期临床甲减危害: 母亲:流产、妊娠期高血压疾病、胎盘早剥、剖宫产、产后出血 胎儿:早产、低出生体重、新生儿呼吸窘迫、神经精神发育异常、胎儿死亡 1.妊娠期临床甲减的诊断标准是血清TSH>妊娠期参考值上限,FT410 mIU/L,无论FT4是否降低,按照临床甲减处理 3.血清TSH治疗目标: 早期TSH 0.1~2.5 mIU/L 中期TSH 0.2~3.0mIU/L 晚期TSH 0.3~3.0mIU/L 一旦确定临床甲减,立即开始治疗,尽早达标。 4.已患临床甲减的妇女计划妊娠,需将TSH控制在妊娠期参考值上限,FT4在正常范围内。 2.妊娠期SCH 增加不良妊娠结局和后代智力发育损害的风险,但由于证据不足,而对TPOAb阴性者既不反对也不推荐治疗。 3.对TPOAb阳性的SCH孕妇建议进行LT4治疗。 4.妊娠期亚临床甲减的治疗方法、治疗目标与监测频度与临床甲减相同,可以根据TSH升高程度,给予不同剂量L-T4治疗 5. L-T4起始剂量根据TSH升高程度选择: 可以通过以下3种方式估算L-T4的需要量: ①妊娠期L-T4的需要量增加30%~50%; ②按每公斤体重计算需要量,即每天2.0~2.4μg/kg(非妊娠期为每天1.6~1.8μg/kg); ③根据测得的血清TSH水平判断L-T4的补充剂量。例如血清 TSH5~10mU/L,补L-T4 25~50μg/d; TSH10~20mU/L,补L-T4 50~75μg/d; TSH>20mU/L,补L-T4 75~100μg/d。 推荐妊娠期血清TSH的治疗目标值T1期<2.5mU/L,T2期和T3期<3.0mU/L;
高淑萍 主治医师 安徽省妇幼保健院 产科1845人已读 - 医学科普 关于超声软指标的相关内容
妊娠15~23周超声检测到胎儿颈部皮肤增厚,是妊娠中期最早发现的超声软指标之一,也是最有预测价值的指标之一。早期研究认为,颈后皮肤厚度≥6 mm提示胎儿染色体异常风险。另有研究利用受试者工作特性曲线进行统计分析,认为在妊娠20周以前,建议以颈后皮肤厚度>5 mm为界值。近期研究发现,颈后皮肤厚度值随着妊娠周数的增加而增大,故需要根据不同妊娠周数制定特异的界值。Smith-Bindman 等研究显示,颈后皮肤增厚会增加21-三体风险,其似然比为17( 95%CI: 8~38)。若妊娠早期胎儿颈项透明层厚度正常,则颈后皮肤增厚的发生率较低。此外,颈后皮肤增厚也可能是胎儿水肿或淋巴水囊瘤的早期表现。染色体异常在活产儿中的发生率为0.1%~0.2%,其中最常见的是21-三体,发生率约为1/800例活产儿,其他包括13-三体、18-三体、X染色体单体、三倍体等。目前有多种手段可用于检测染色体异常,包括生物化学指标、羊膜腔穿刺染色体核型分析以及超声检查。羊膜腔穿刺染色体核型分析的结果较为准确,但介人性操作可能导致0.5%~1.0%的胎儿死亡风险。 妊娠18~24周进行的妊娠中期超声检查,可以发现一些明确的胎儿结构异常和超声软指标。超声软指标并不特异,常为一过性存在,在正常胎儿中可见,但在染色体异常的胎儿中其发生率升高。目前研究较充分的超声软指标包括:脉络丛囊肿、心内强回声、颈后皮肤增厚、肠管强回声、肾盂扩张、长骨短、鼻骨缺损或发育不良、轻度侧脑室增宽和单脐动脉等。超声软指标并非病理性指标,但可用于评估染色体异常的风险。 一、超声软指标的表现与临床意义 1.脉络丛囊肿:脉络丛囊肿在胎儿头颅的轴面可见,位于侧脑室,可为单发或多发,单侧或双侧,表现为脉络丛内的局限性无回声区。如果仅存在脉络丛囊肿1项软指标,并不能提示染色体异常的风险增高。当超声检查发现合并其他结构异常时,胎儿18-三体的风险增高,但21-三体的风险并不增高。正常妊娠中1%-2.5%的胎儿可出现脉络丛囊肿。 Chitty等的大规模多中心研究随机选取1 600例孕妇,其中658例胎儿存在脉络丛囊肿,其染色体异常(主要为18-三体)的风险为对照组的1.5倍。Comstock研究显示,49 435例妊娠16~25周的孕妇行超声检查,发现胎儿脉络丛囊肿1 209例(2.3%),其中1060例仅有脉络丛囊肿而不合并其他结构异常;最终确诊50例18-三体胎儿,其中一半存在脉络丛囊肿。该研究认为,发现胎儿脉络丛囊肿后,需要仔细检查胎儿其他结构,尤其是双手,以发现有无重叠指和紧握拳,辅助除外18-三体。如果胎儿不合并其他结构异常,则18-三体的风险不会增高;如果伴随其他结构异常,建议行羊膜腔穿刺染色体核型分析。 2.心内强回声:心内强回声指在乳头肌或任意心室内出现的回声与骨质强度类似的微小钙化灶,可存在于单一心室或双心室,可单发也可多发。超声检查时应注意,必须从多个角度可她才可判定为心内强回声,以除外乳头肌的镜面反射回声。1.5%~4%的胎儿中可见心内强回声。假性心内强回声常出现的位置包括调节束、心内膜垫和三尖瓣环。 为了正确识别心内强回声,推荐方法如下:(1)存在乳头肌的心室内;(2)从多个平面角度可见;(3)独立于乳头肌镜面反射区;(4)不应表现为入-出口反射。 Coco等总结12 672例妊娠中期孕妇的超声检查结果,认为胎儿心内强回声不增加其染色体异常的风险。Filly等研究显示,21 839例21-三体低风险孕妇中,626例(2.9%)胎儿仅存在心内强回声,其中仅1例胎儿患21-三体。Rochon和Eddleman研究显示,在染色体异常低危群体中,仅心内强回声1项指标与21-三体无相关性,即使存在风险,也远低于行介入性产前诊断带来的胎儿丢失风险,故年龄不足35岁的孕妇超声发现胎儿心内强回声是正常生理表现,不建议行羊膜腔穿刺。 发现典型的心内强回声后,需要对胎儿进行细致的超声检查,以明确有无结构异常,如果合并其他明显的结构异常或软指标,建议行羊膜腔穿刺术。 3.颈后皮肤增厚:妊娠15~23周超声检测到胎儿颈部皮肤增厚,是妊娠中期最早发现的超声软指标之一,也是最有预测价值的指标之一。早期研究认为,颈后皮肤厚度≥6 mm提示胎儿染色体异常风险。另有研究利用受试者工作特性曲线进行统计分析,认为在妊娠20周以前,建议以颈后皮肤厚度>5 mm为界值。近期研究发现,颈后皮肤厚度值随着妊娠周数的增加而增大,故需要根据不同妊娠周数制定特异的界值。 Smith-Bindman 等研究显示,颈后皮肤增厚会增加21-三体风险,其似然比为17( 95%CI: 8~38)。若妊娠早期胎儿颈项透明层厚度正常,则颈后皮肤增厚的发生率较低。此外,颈后皮肤增厚也可能是胎儿水肿或淋巴水囊瘤的早期表现。 4.肠管强回声:1990年,Nyberg等和Persutte最早报道了胎儿肠管强回声。妊娠中期超声检查发现胎儿肠管回声与临近骨质回声一致时,方可诊断肠管强回声。肠管强回声可分为局灶、多灶或弥散强回声3种。检查胎儿肠管强回声时,探头频率不应高于5 MHz.一旦可疑肠管强回声,应逐渐降低超声增益,直至只可见骨和肠管为止。 有学者提出肠管强回声的分级方法,用于减小不同检查者之间的差异。Slotnick和Abuhamad将肠管强回声与髂嵴回声强度对比,分为3级:1级指肠管回声强度低于髂嵴;2级指肠管回声强度与髂嵴相同;3级指肠管回声强度高于髂嵴。2级和3级肠管强回声与染色体非整倍体和不良妊娠结局的关系更密切。 妊娠中期肠管强回声的发生率为0.2%~1.4%。胎儿正常、胎儿染色体异常、胎儿生长受限、妊娠早期出cf、囊性纤维化、先天性病毒感染或地中海贫血等情况下均有可能发生。Bromley等研究发现,妊娠中期仅0.6%的胎儿可见肠管强回声;但21-三体胎儿中约15%存在肠管强回声。Sepulveda和Sebire研究发现,肠管强回声胎儿中,约35%存在病理改变。 妊娠早期出血时,由于胎儿吞人血液,也可能导致肠管强回声。如果发现肠管强回声,需要对胎儿进行细致检查,建议行羊膜腔穿刺,以确定染色体核型以及有无巨细胞病毒、弓形虫和细小病毒感染,并应同时检查母体是否近期有巨细胞病毒和弓形虫感染。因可能同时存在胎儿生长受限,推荐行动态超声监测。 5.肾盂扩张:妊娠中期胎儿肾盂扩张较为常见,发生率为0.3%~4.5%(平均约为1%)。轻度肾盂扩张指肾盂宽度在4~10 mm之间,且不存在肾盏扩张。肾盂宽度≥10 mm或肾积水的胎儿有结构异常的风险,需要继续评估。 1990年,Benacerraf等首先发现肾盂扩张与染色体异常有关,21-三体胎儿和正常胎儿发生轻度肾盂扩张的比例分别为25%和2.8%。Chudleigh等的前瞻性多中心研究显示,101 600例孕妇行超声检查,发现737例胎儿存在轻度肾盂扩张,其中12例(1.6%,12/737)有染色体异常(9例合并其他超声指标异常,1例孕妇高龄,2例仅有轻度肾盂扩张l项异常),认为胎儿在仅有轻度肾需扩张而不合并其他异常时,孕妇年龄
高淑萍 主治医师 安徽省妇幼保健院 产科5281人已读





